Sevgili okurlar; sizlere ilköğretim, ortaöğretim ve liselerde öğrencilerin korkulu rüyalarından biri olan ödev, performans ödevi ve proje ödevleri hakkında yardımcı olmak istedik. Öğretmenlerimizin öğrencilerin ders işleyişini, derse katılımını ve başarı oranlarını arttırabilmek adına verdikleri bu ödev şekilleri hemen hemen bütün dersler için verilmektedir. Ödev hemen hemen her hafta verilmekteyken performans ve proje ödevleri ise dönem sonu veya belli aralıklarla öğrencilere verilmektedir. Peki bu ödevlerin konularından biri olan periyodik cetvel nedir konusuna gelirsek, öğrencilerin kafalarında birden fazla soru işareti gelmektedir. Öğretmenler öğrencilere verdikleri periyodik cetvel nedir sorusunun yanı sıra periyodik cetvelin tarihçesini de sormaktadır. İşte bizde sizlere bu konular hakkında yardımcı olmaya çalışacağız.
Periyodik Cetvel Nedir?
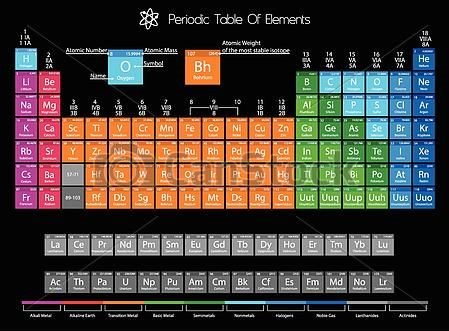
Bilinen tüm elementler, artan atom numaralarına göre sıralandırılarak bir liste oluşturulur. Liste, benzer özelliğe sahip elementler bir araya gelecek şekilde düzenlenir. 1869 yılında Mendeleyev’in o dönemde bilinen tüm elementleri atom kütlelerinin büyüklüğüne göre sıralayarak oluşturduğu listeye periyodik cetvel denir.
Periyodik Tablo Nedir?
Periyodik tablo, kimyasal elementlerin sınıflandırılması için geliştirilmiş tablodur. Dilimizde periyodik tablo, periyodik cetvel, periyodik çizelge, elementler tablosu gibi birçok şekilde isimlendirilmiştir. Bu tablo bilinen bütün elementlerin artan atom numaralarına göre bir sıralanışıdır.
Periyodik Cetvelin Özellikleri Nedir?
Periyodik tablo soldan sağa doğru 1A grubundan başlar ve 8A grubuna kadar sıralanır. Bu sıralama elementlerin metal, ametal, yarı metal olma durumuna göredir.
- 1A grubu Alkali Metallerdir.
- 2A grubu Toprak Alkali Metallerdir.
- 3A grubu Toprak Metalleridir.
- 7A grubu Halojenlerdir.
- 8A grubu Soygazlardır.
- B grubu ise geçiş metalleridir.
Periyodik cetvelde yukarıdan aşağı doğru inildikçe;
- Atom numarası ve metalik özellik artar.
- Elektron sayısı artar ancak ametallik özellik azalır.
- Atop çapı büyür ve kütle numarası artar.
Periyodik Tablo üzerinde soldan sağa doğru gidildikçe;
- Atom numarası ve kütle numarası artar.
- Elektron sayısı artar ancak metalik özellik azalır.
- Atom çapı büyür ve kütle numarası artar.
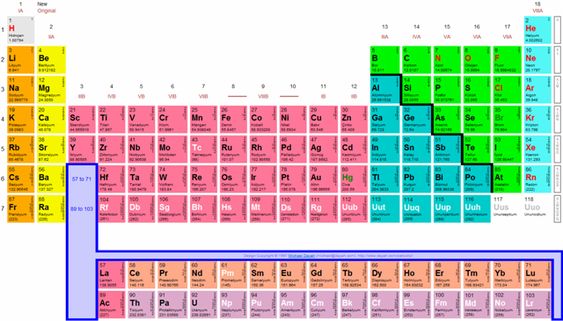
Periyodik Cetvelin Tarihçesi Nedir?
Altın, gümüş, kalay, bakır, kurşun ve cıva demir gibi elementler eski çağlardan beri biliniyordu. Bir elementin ilk bilimsel olarak bulunması 1649 yılında Henning Brand’ın fosforu bulmasıyla başlamıştır. Bundan sonraki 200 yıl boyunca elementler ve onların bileşikleri hakkında kimyacılar tarafından pek çok bilgi elde edilmiştir. Bununla beraber 1869 yılına kadar toplam 63 element bulunabilmiştir.
1817 yılında Johann Dobereiner benzer kimyasal özelliklere sahip olan stronsiyum, kalsiyum ve baryuma bakarak, stronsiyumun atom ağırlığının kalsiyum ve baryum atom ağırlıklarının ortasında olduğuna dikkat çekmiştir. Periyodik cetvelin 1829 yılında klor, brom ve iyot üçlüsünün de benzer özellikler gösterdiği bulunmuştu. Yine benzer davranış lityum, sodyum ve potasyum için de gözleniyordu. 1829 ve 1858 yılları arasında bu konuda pek çok araştırma yapıldı. Bu sırada halojenler grubu katıldı. Oksijen, kükürt, selenyum ve tellür bir grubun üyesi olarak düşünülürken azot, fosfor, arsenik, antimon ve bizmut başka bir grup içine yerleştirildiler.
İlk periyodik tabloyu oluşturma şerefi Fransız bilim adamı A. E. Beguyer de Chancourtois’e düştü. De Chancourtois, silindirin çevresine 16 kütle birimleri yerleştirerek element ve iyonları buraya oturttu. Benzer özelliklerdeki elementler bu silindir üzerinde düşey satırlarda gruba ayırmıştı. Atom ağırlıkları sekizin katı kadar olan elementlerin özellikleri benzerdi. 1864 yılında yazılan bir yazıda Newlands bunu Oktav kanunu (Law of Octaves) olarak tanımladı. Bu kanuna göre herhangi bir element tablodaki sekizinci elementle benzerlikler gösteriyordu.
Genelde periyodik tablonun babası olarak Alman bilim adamı Julius Lothar Meyer ve Rus bilim adamı Dimitri Mendeleyev kabul edilir. Her ikisi de birbirinden habersiz olarak dikkate değer benzer sonuçlar ürettiler. Mendeleyev atomların artan atom ağırlıklarına göre sıralandıklarında belli özelliklerin tekrarlandığını görmüştür. Daha sonra elementleri tekrarlanan özelliklerine göre alt alta sıralayarak ilk iki periyodu yedişer, sonraki üç periyodu ise onyedişer element içeren bir periyodik sistem hazırlamıştır. Mendeleyev’in hazırladığı periyodik sistemde bazı yerleri henüz keşfedilmemiş elementlerin olduğunu düşünerek boş bırakmıştır. Daha sonra bulunan skandiyum, galyum, germanyum elementleri tablodaki boşluklara yerleşmişlerdir.
Periyodik cetvelin tarihçesi hakkında 1895 yılında Lord Rayleigh, yeni bir soygaz (argon) keşfettiğini bildirdi. Bu element periyodik tabloda bilinen hiçbir yere oturtulamadı. 1898 yılında William Ramsay bu elementin klor ile potasyum arasında bir yere konulabileceğini önerdi. Helyum da aynı grubun bir üyesi olarak düşünüldü. Bu grup elementlerinin değerliklerinin sıfır olması nedeniyle sıfır grubu olarak adlandırıldı.
Mendeleyev’in periyodik tablosu her ne kadar elementlerin periyodik özelliklerini gösterse de neden özelliklerin tekrarlandığı konusunda herhangi bir bilgi vermemektedir.

Periyodik Tablo Nasıl Okunur?
Bunun görmek için Kalsiyum (Ca) atomunu ele alalım. Periyodik tabloya baktığımız zaman, kalsiyum simgesinin üstünde atom numarasını (20) ve hemen altında da element ağırlığını (40) görüyoruz ki bu hesaplamaya genellikle elektronları katmıyoruz.
Kısacası 20 sayısı kalsiyum atomundaki proton sayısı ve 40 sayısı da proton ile nötron sayısının toplamı oluyor. Biz de periyodik tabloda üstteki sayıyı (20), alttaki sayıdan çıkardığınız zaman (40), o atomun nötron sayısını buluyoruz.
Keza plütonyumun atom numarası 94 ve bağıl atom kütlesi de 244’tür. Kütle sayısını da bazen yuvarlıyoruz. Mesela kalsiyum atomunun bağıl kütle sayısı aslında 40 değil, 40,078(4).
Periyodik Tabloda Kaç Element Vardır?
Fizikçiler 1930’dan bu yana doğada olmayan yeni elementler keşfediyor ve bugün periyodik tabloda 118 element yer alıyor.
Performans/Proje Ödevleri;